| Tovholder: Birte Nygaard (This email address is being protected from spambots. You need JavaScript enabled to view it.) Udarbejdelse: Oktober 2012 Næste revision: Oktober 2015 |
Thyrotoksikose
Definition
I praksis bruges begreberne hyperthyroidisme, hyperthyreose og thyrotoksikose ofte som synonymer, men thyrotoksikose defineres som en øget forekomst af thyroideahormon i blodet, mens hyperthyroidisme/hyperthyreose defineres som en øget produktion af thyroideahormon fra gl. thyroidea.![]()
Forekomst
I Danmark diagnosticeres årligt 80/100.000 svarende til ca. 5.000 nye tilfælde af hyperthyroidisme. Kvinde- mand ratio 5:1. Diffus toksisk struma ses hyppigst hos unge og multinodøs/nodøs toksisk struma ses med stigende forekomst efter 50 års alderen (1). Livstidsrisiko i Danmark er 10,5 % for kvinder og 2,4 % for mænd (2).![]()
Figur 1. Diagnostisk algoritme baseret på målinger af TSH, T3 og T4
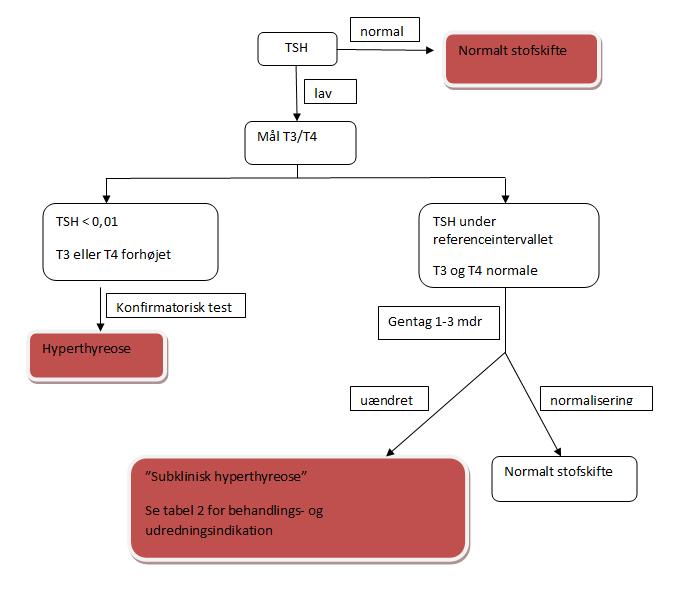
Symptomer
Kan være diffuse og variere i sværhedsgrad, bl.a. afhængig af alder og co-morbiditet. Nedenstående er ikke udtømmende, og man behøver ikke have alle symptomer:
Indre uro, nervøsitet, søvnbesvær, koncentrationsbesvær, hukommelsesbesvær, hjertebanken, åndenød, tremor, vægttab, diarré, menstruationsforstyrrelser, varmeintolerans og hedeture, træthed, struma.![]()
Komplikationer
Osteoporose, atrieflimren, hjertesvigt, kognitive deficit samt øget mortalitet.![]()
Udredning
Ved mistanke om stofskiftelidelse måles som screeningsprøve TSH. Er denne abnorm måles T4 og T3.
Patienter henvist med Thyrotoksikose udredes med:
- TSH, frit-T4 (FT4), FT3 (eller total T4, T3 og mål for thyroxinbindende globulin).
- SR/CRP ved mistanke om thyroidit.
- TSH-receptor antistoffer (TRAb).
- Thyroideascintigrafi/ultralyd (afhængig af lokale retningslinjer anvendes scintigrafi eller ultralyd som primær billeddiagnostik).

Thyrogen
Autoimmun
Non-autoimmun
- Multinodøs toksisk struma
- Solitært toksisk adenom
- HCG-overproduktion
Betinget af destruktion af glandula thyroidea: (Beskrives i særskilt NBV)
- Subakut thyroiditis (De Quervain)
- Stum thyroiditis (inklusive postpartum thyroiditis)
- Thyroiditis efter radiojodbehandling
Farmakologisk betinget (Beskrives i særskilt NBV)
- Amiodaron
- Jod excess – såsom røntgen kontrast
- Excessiv thyroideahormon indtagelse (thyrotoxicosis factitia)
- Immunmodulerende stoffer
- Lithium
Sekundær hyperthyroidisme ved hypofyse/hypothalamuslidelser
- TSH-producerende hypofyseadenom (sjælden)
Non-thyroidea sygdom
- Svær somatisk eller psykiatrisk sygdom kan medføre påvirket thyroidea funktion - typisk ses primært lavt s-T3, men TSH kan også være supprimeret
|
Graves sygdom |
|
|
Multinodøs toksisk struma |
|
|
Solitært toksisk adenom |
|
|
Subakut thyroidit |
|
|
Medikamentel/jod betinget thyroidit |
|
- Subklinisk thyrotoksikose
- Overt/åben Thyrotoksikose
- Thyrotoksisk krise
Diffus toksisk struma (Graves’ sygdom) ICD-10 E05.0:
Synonymer: Diffus toksisk struma, Graves’ sygdom, Mb. Basedow.![]()
Ætiologi:
Graves’ sygdom er en autoimmun sygdom, hvor forekomsten af antistoffer mod TSH receptoren (TRAb) bevirker forhøjet stofskifte, evt. struma og øjensymptomer – Graves’ Orbitopati, tidl. benævnt thyroidea associeret ophthalmopati (TAO).![]()
- Antithyroid medicin
- Radioaktivt jod
- Thyroidektomi
I Danmark er der tradition for medicinsk behandling, som fører til remission hos op til 50-60 % af patienterne, men behandlingsmodaliteterne er principielt ligeværdige under hensyntagen til bl.a. risikoen for komplicerende Graves' Orbitopati,. Ved sygdomsrecidiv eller patientpræference herfor bør en definitiv behandling med Radioaktivt jod eller operation overvejes. Hos ældre med betydende co-morbiditet kan langtidsbehandling med antithyroid medicin overvejes.
Efter ophør med antithyroid behandling er recidiv risikoen er størst hos rygere, mænd, høj TRAb, initialt svær T3 forhøjelse og stor struma.
Særlige hensyn i forhold til behandlingsvalg gælder for patienter med Graves’ Orbitopati, gravide/ammende og børn (beskrives i særskilt NBV).
Livskvaliteten (QoL) er ofte nedsat hos patienterne med klager over en fornemmelse af ”ikke at være sig selv”, selv når stofskiftet biokemisk er normaliseret. Imidlertid er QoL sammenlignelig ved hver af de tre behandlingsmuligheder. (3)
Der udspørges og undersøges specifikt for Graves’ Orbitopai, og patienten oplyses om symptomer herpå, der bør føre til prompte lægekontakt; specielt vedvarende synsnedsættelse, øjensmerter eller påvirket farvesyn.
Ved valg af behandling bør patienten inddrages i fordele og ulemper ved de forskellige regimer.![]()
Symptomatisk behandling
Bør overvejes hos alment påvirkede patienter særligt ældre patienter med hvilepuls over 90 eller kendt hjertesygdom.
- Propranolol er førstevalg, dosering 10-40 mg x 4 dagligt. Udtrappes over 1 uge, når patienten er euthyroid.
- Ved kontraindikationer til Propranolol kan Verapamil, vælges i dosering 40-80 mg x 3 dagligt.
- Rygestop
- Tilrådes, da rygning øger risikoen for recidiv og for udvikling af Graves’ Orbitopati.
Antithyroid behandling
Som udgangspunkt opstartes alle patienter initialt i antithyroid medicinsk behandling.![]()
Medicinsk behandling
Vælges i håb om at opnå remission. Der behandles med titrerings-regime eller block-replacement-terapi .
Titrerings-regime foretrækkes ofte pga. lavere antithyroid medicinsk dosis og dermed mindre risiko for bivirkninger.
Block-replacement-terapi vælges når behovet for stabilt stofskiftekontrol vægtes højt, fx ved Graves’ Orbitopati, eller hvis behandling med titrering viser sig vanskelig (svingende stofskifte).
Block-replacement-terapi er kontraindiceret hos gravide.
Førstevalg antithyroid medicin er Thiamazol – pga. lavere risiko for bivirkninger sammenlignet med Propylthiouracil (PTU). Behandlingsvarighed er vanligvis 12-18 måneder. Block-replacement-terapi kan seponeres umiddelbart eller udtrappes under fortsat L-thyroxin behandling .
Ved moderat til svær Graves’ Orbitopati vil medicinsk behandling være 1. valgs behandling. (4)
- Kløende hududslæt.
- Ledsmerter.
- Agranulocytose ca. 1 %, oftest < 100 dage, men kan opstå sent i forløbet: Ved feber eller halssmerter skal pt. pausere Thiamazol og søge læge mhp. kontrol af leukocyt-differentialtælling. Neutropeni bør føre til skift af behandlingsstrategi.
- Leverpåvirkning, oftest cholestatisk: vedvarende mavesmerter, kvalme, anoreksi, icterus, lysfarvet afføring og mørk urin skal føre til lægekontakt mhp. kontrol af leverparametre.
Patienten skal ved behandlings start informeres om bivirkninger til antihyroid medicin specielt forholdregler vedr. feber.
Der er ikke kryds-allergi mellem thiamazol og PTU, om end en kraftig allergisk reaktion giver en større risiko for allergi mod begge præparater.
Bivirkningerne opstår hyppigst ved høj dosis men kan også ses ved lav dosering.
Målet for behandlingen er, at stofskiftet ligger højt i normalområdet, dvs. T4 i normalområdet og TSH nederst i normalområdet, når denne atter er målbar (ofte først efter måneder).
Det er helt centralt at undgå TSH forhøjelse, da Graves’ Orbitopati herved kan forværres eller fremprovokeres.
Kontrol efter f.eks. 3 og 6 uger, 3, 6 og 12 mdr.
Der behandles som hovedregel i 12-18 måneder.
Opfølgning efter endt behandling:
Kontrol f. eks. efter 3 og 6 uger, 3,6 og 12 måneder. Patieten afsluttes til egen læge med råd om
- Kontrol af stofskiftet årligt eller ved symptomer på hyperthyroidisme.
- Lægehenvendelse ved øjensymptomer.
Ved graviditet kræves ekstra kontrol (se i øvrigt NBV graviditet og thyroideasygdom - følger)![]()
Radioaktiv jodbehandling, (se i øvrigt NBV Radioaktiv jodbehandling – følger)
Overvejes ved recidiv efter medicinsk behandling eller som initial behandling ved ønske om definitiv behandling, fx ved stor struma. Behandlingens succeskriterium er at gøre patienten eu- eller hypothyroid.
Det er forventeligt, at en stor del af patienter med Graves’ vil udvikle hypothyroidisme efter behandlingen pga. optagelse af radioaktiv jod i hele kirtlen.
Symptomatisk behandling med betablokade ved behov.
Eventuel antithyroid forbehandling: Der anvendes monoterapi og stiles mod stofskifte højt i normalområdet med lav/suprimeret s-TSH, for at opnå den mest optimale effekt af Radioaktiv jodbehandling. Behandlingen pauseres før og genoptages efter individuel vurdering efter Radioaktiv jodbehandling i henhold til lokal vejledning – feks 4 dage før og 7 dage efter.
Husk evt planlægning af steroid profylakse- se neden for.
Specielt ved Graves’ er ændringerne i stofskiftet uforudsigelige efter Radioaktiv jodbehandling, idet der kan ses hurtig udvikling af hypothyroidisme, men også længerevarende stigning i stofskiftet med samtidig stigning i TRAb kan ses.
Strålethyroidit forekommer indenfor de første uger med forbigående forværring af det høje stofskifte. Behandles symptomatisk.
Strumasvind på 50 % opnås, oftest indenfor 6 mdr. Fuld effekt ses efter 12 mdr.
F. eks. efter 3 og 6 uger og 3, 6 og 12 måneder.
Det videre forløb afhænger af thyroidea status
- Er pt. euthyroid afsluttes til egen læge med råd om årlig stofskiftekontrol grundet stor risiko for myksødem. Ved komplicerede tilfælde eller ønske om snarlig graviditet kan pt. evt. følges længere.
- Er pt. hypothyroid afsluttes til fortsat kontrol hos egen læge, når substitutionsbehandlingen med L-thyroxin er indstillet.
- Er pt. vedvarende eller atter hyperthyroid kan Radioaktiv jodbehandling gentages, tidligst 4 måneder efter første behandling. Fertile kvinder skal instrueres i behovet for kontrol af stofskifte før og under graviditet (se NBV graviditet og thyroideasygdom).
- Radioaktiv jodbehandling øger risikoen for udvikling eller forværring af Graves’ Orbitopati. Ved valg af Radioaktiv jodbehandling bør man vurdere patientens øvrige risikofaktorer (rygning, høj TRAb, initial høj T3) for udvikling af Graves’ Orbitopati. Hos patienter med aktiv, mild Graves’ Orbitopati anbefales samtidig binyrebarkhormon behandling (typisk 30 mg dgl i 4 uger, med efterfølgende nedtrapning) (5)
Graviditet, amning, manglende compliance til strålehygiejniske forholdsregler, aktiv og moderat til svær Graves’ Orbitopati, graviditetsønske indenfor 4 måneder.
Ulemper
Risikoen for behandlingssvigt er dosisafhængig. De fleste udvikler hypothyroidisme og får behov for substitutionsbehandlings med L-thyroxin. Risiko for udvikling eller forværring af Graves’ Orbitopati. Graviditet frarådes hos både kvinder og mænd i perioden 4 måneder efter Radioaktiv jodbehandling.![]()
Operation (Se NBV thyroidea kirurgi – følger)
Vælges ved ønske om hurtig og endelig stofskiftekontrol, særligt ved stor symptomgivende struma, cancermistanke, gentagne recidiver eller moderat til svær Graves’ Orbitopati. Der anbefales total thyroidektomi mhp. at undgå recidiv. Der er derfor efterfølgende livslangt behov for thyroideahormonsubstitution. Operation er mere effektivt end Radioaktiv jodbehandling, idet der ikke opstår recidiv af hyperthyroidisme.
Der forbehandles med antithyroid medicin og evt. betablokker. Der stiles så vidt mulig efter normalisering af stofskiftet før operation. Er dette ikke muligt pga. f.eks. medicinallergi, stiles mod betablokkering (evt. anvendelse af verapamil) til puls ca. 80. Ved svær hyperthyroidisme kan anvendes peroral kalium-iodid mikstur mhp. blokering af kirtlen og herved reduktion af stofskiftet. Dosis f.eks. Kalium-jodid mikstur, 20 mg/ml, 10 ml dagligt i 10 dage forud for operation.
Kontraindikationer
Betydende co-morbiditet, graviditet (relativ) (se NBV graviditet og thyroideasygdom).
Komplikationer til kirurgi
Per- og post-operativ blødning, infektion, n. recurrens parese (ca. 1 %), hypoparathyroidisme (5 % - 10 %)
Opfølgning
Indstilling af substitutionsbehandling og kontrol af Ca2+ efter behov.![]()
Toksisk multinodøs struma ICD-10: E05.2
Synonymer: Knude-struma med højt stofskifte, Toxic multinodular goitre, Plummers disease.![]()
Tilstanden skyldes, at der i glandula thyroidea opstår autonomt fungerende celler. Sådanne celler har typisk en aktiverende somatisk mutation i TSH receptoren, hvilket kan medføre både struma og hyperthyroidisme. Jodmangel er en væsentlig risikofaktor for opståen af autonomi. Tilstanden er oftest langsomt progredierende og livslang.![]()
Symptomerne på hyperthyroidisme er ofte milde, eventuelt fraværende. Der kan være strumarelaterede symptomer som globulusfornemmelse, synkebesvær eller kosmetiske gener. Struma er ofte med sideforskel og palpable knuder.
Mild hyperthyroidisme er forbundet med risiko for atrieflimren og osteoporose og er af denne grund behandlingskrævende uanset eventuel manglende symptomatologi.![]()
Se under hyperthyroidisme og differentialdiagnostiske overvejelser.![]()
Der findes tre behandlingsformer (+ evt symptom behandling se under Graves’ sygdom):![]()
(Se iøvrigt særskilt NBV om Radioaktiv jodbehandling – følger)
131Jod optages fortrinsvis i autonome thyrocytter, der uger til måneder efter behandling ødelægges. Ved Radioaktiv jodbehandling er effekten på hyperthyroidisme langsomt indsættende, idet ca. 50 % af patienterne er euthyroide efter 3 mdr. og 80 % efter 6 mdr. Effekt på struma er ofte varierende (gennemsnitligt 40 % - 50 % struma reduktion) og mere langsomt indsættende (ændringer kan stadig ses 1-2 år efter) (6) . Risiko for hypothyroidisme hos ca. 30% af patienterne i løbet af de første 5 år.
Hos ældre eller hjertesyge patienter anvendes antithyroid medicin som forbehandling til Radioaktiv jodbehandling for at opnå hurtig stabilisering af stofskiftet og for at undgå opblussen umiddelbart efter Radioaktiv jodbehandling .
Kontraindikationer og komplikationer
Se under Graves’ Sygdom.
Opfølgning
Regelmæssig kontrol af TSH og T4 mhp. udvikling af thyroidit og/eller hypothyroidisme.![]()
Ved stor struma og især ved kompression af trachea foretrækkes operativ behandling. Der bør udføres total (nær-total) thyroidektomi.
Komplikationer og opfølgning
3) Medicinsk antithyroid behandling.
Denne behandling er grundet sygdommens naturhistorie livslang med risiko for bivirkninger. Kan anvendes i lav dosering til ældre eller svagelige patienter, der ikke kan eller ønsker at medvirke til Radioaktiv jodbehandling eller operation.
Opfølgning
Regelmæssig kontrol af TSH og T4 mhp. Behandlingsjustering, fx hver 8 uge. Efter stabilisering kan patienten afsluttes til egen læge, med kontrol hver 3.-6. måned. Behandling og kontrol er livslang.![]()
Supplerende:
Scintigrafisk ”kolde knuder” ved Toksisk multinodøs struma udredes og behandles i henhold til vejledning for dette (se NBV udredning af knuden i gl. thyroidea).
Patienter med Graves’ og samtidig toksisk multinodøs struma behandles primært som Graves sygdom. Hvis antithyroid medicin ikke kan udtrappes eller der opstår recidiv vælges efterfølgende Radioaktiv jodbehandling eller kirurgi.![]()
Solitært toksisk adenom ICD-10: E05.1
Se afsnittet om multinodøs toksisk struma for baggrunden for opståen af autonomi. Solitær toksisk adenom adskiller sig fra multinodøs toksisk struma, ved at der kun er et enkelt adenom med autonom hormon produktion. Ligesom multinodøs toksisk struma er tilstanden oftest langsomt progredierende og livslang. Forekomsten af Solitær toksisk adenom er ikke relateret til jodstatus.![]()
Oftest symptomfattig, men alle symptomer på hyperthyroidisme kan ses.![]()
Se under hyperthyroidisme samt differentialdiagnostiske overvejelser.![]()
Se tabel 1.![]()
Som multinodøs toksisk struma.![]()
(Se i øvrigt særskilt NBV om Radioaktiv jodbehandling – følger):
Radioaktivt jod er normalt den anbefalede behandling. Effekten på hyperthyroidismen er bedre for Solitært toksisk adenom end ved multinodøs toksisk struma, idet der er en 75 % respons rate efter 3 mdr. I Danmark bruges relativt lave 131I doser, og behandlingskrævende hypothyroidisme ses hos cirka 10 % 5 år efter radiojod behandling (7). Risikoen for hypothyroidisme er størst hos ældre og hos patienter, der ikke havde supprimeret TSH før behandling.![]()
Medikamentel antithyroid behandling benyttes efter samme principper som ved multinodøs toksisk struma. Se afsnittet herfor.![]()
Ved kirurgi foretages hemithyroidektomi.![]()
Scintigrafisk ”kolde knuder” udredes i henhold til vejledningen herfor (NBV: Udredning af knuden i gl. thyroidea), og før man eventuelt vælger Radioaktiv jodbehandling .
Subklinisk thyrotoksikose
Definition
Subklinisk thyrotoksikose er ikke en selvstændig sygdomstilstand men hentyder til sygdomsgraden. Ætiologi og udredning er derfor som for thyrotoksikose generelt.
Det er en biokemisk diagnose, der stilles, når TSH ved gentagne målinger er under referenceområdet og T4 og T3 er normale. Typisk vil FT4 og FT3 dog ligge højt i normalområdet.
Det forudsættes, at patienten ikke er svært kronisk eller akut syg (non-thyroidal illness).![]()
Prævalensen af subklinisk thyrotoksikose afhænger af alder, køn og jodindtaget. Subklinisk thyrotoksikose rammer 10 % af befolkningen i jodmangel områder og ca. 1% i jodsufficiente områder (8). Tilstanden forekommer hyppigere med stigende alder.![]()
Anden sygdom eller farmakologisk behandling, fx med glukocorticoider, kan give et lignende biokemisk billede. Se i øvrigt tabel 1.![]()
Oftest asymptomatisk, men forbundet med risiko for komplikationer såsom atrieflimren og osteoporose. Patienterne bør udredes for dette.![]()
Indikation for behandling er omdiskuteret. Der er styrket indikation for behandling ved s-TSH < 0,1mU/L og alder > 65 år, eller tilstedeværelse af symptomer heniblandt hjertesygdom inklusiv atrieflimren og osteoporose. Forslag til behandling kan følge nedenstående tabel.
Valg af behandlingsmodalitet afhænger af ætiologien.![]()
Tabel 2: Behandlings- og udredningsindikation (9)
| TSH < 0,1 mU/L | |
| Alder > 65 år | Ja |
|
Alders < 65 år, med risikofaktorer:
|
|
| Alder < 65 år, uden risikofaktorer: | Overvej |
Ubehandlede bør kontrolleres hver 6-12 mdr – kan følges hos egen læge.![]()
Thyrotoksisk krise
Diagnose
Sjælden, livstruende tilstand med svære thyrotoksiske symptomer. De klassiske symptomer er takycardi/arytmitendens, feber og cerebral påvirkning. Herudover kan der ses diarré, kvalme, opkastninger, dehydrering, kardiel inkompensation, tendens til tromboembolisme og cirkulatorisk kollaps. Tilstanden er ofte præcipiteret af anden sygdom, traume, operation eller fødsel hos patient med uerkendt eller insufficient behandlet hyperthyroidisme.
Diagnosen baseres på kliniske fund, idet de perifere thyroideahormoner ikke nødvendigvis findes svært forhøjede.![]()
Behandlingen forgår ofte på intensiv afdeling.
Antithyroid behandling
Propylthiouracil (PTU) foretrækkes da PTU i høje doser hæmmer den perifere omdannelse af T4 til T3.
Der gives en bolus på 400 mg PTU og herefter 200 mg hver 4.time (knuste tabletter opslemmes i vand og gives peroralt eller i ventrikelsonde). Alternativt kan vælges PTU til iv-dosering. Hvis PTU er kontraindiceret, kan imidazolderivat anvendes.
Jodidindgift
De første 2 døgn gives én time EFTER hver PTU dosis 5 ml Natrium-jodid 50mg/ml iv. Alternativt kan anvendes tbl./mikstur Kalium-jodid 400mg.
Betablokade
Tbl. Propranolol gives i døgndoser på 120-240 mg fordelt på 4-6 doser. Eventuelt gives 2 mg propranolol som langsom iv injektion med 4-6 timers interval under monitorering.
Glukocorticoider
Hydrokortison (Solu-Cortef) 100 mg x 3-4 iv/døgn i 2-3 døgn.
Øvrig behandling:
Hyperpyreksi: Paracetamol og evt. mekanisk afkøling. På sigt overvejes thyroidektomi.
Væskesubstitution
Antibiotika anvendes på vide indikationer.
Yderligere intensivt understøttende terapi afhængig af symptomatologi og udløsende årsag.![]()
- Bulow PI, Laurberg P, Knudsen N, Jorgensen T, Perrild H, Ovesen L, Rasmussen LB.
Increase in incidence of hyperthyroidism predominantly occurs in young people after iodine fortification of salt in Denmark.
J Clin Endocrinol Metab 2006;91:3830-34 - Carlé A, Pedersen IB, Knudsen N, Perrild H, Ovesen L, Rasmussen LB, Laurberg P.
Epidemiology of subtypes of hyperthyroidism in Denmark: a population-based study.
Eur J Endocrinol. 2011;164(5):801-9. - Abraham-Nordling M, Torring O, Hamberger B, et al.
Graves' disease: a long-term quality-of-life follow up of patients randomized to treatment with antithyroid drugs, radioiodine, or surgery.
Thyroid. 2005 Nov;15(11):1279-86. - Abraham P, Avenell A, McGeoch SC, Clark L, Bevan JS.
Antithyroid drug regimen for treating Graves' hyperthyroidism.
Editorial Group: Cochrane Metabolic and Endocrine Disorders Group. Published Online: 20 JAN 2010 on http://www.thecochranelibrary.com - Bartelena L,Marcocci C, Bogazzi F, et al.
Relation between therapy for hyperthyroidism and the course of Graves’ ophthalmopathy.
New Engl J Med 1998;338:73-78 - Nygaard B, Hegedüs L, Nielsen KG, Ulriksen P, Hansen JM.
Radioiodinetreatment of multinoular toxic goitre.
Archives of internal medicine 1999; 159:1364-1368 - Nygaard B, Hegedüs L, Nielsen KG, Ulriksen P, Hansen JM.
Long term effects of radioactive iodine on thyroid function and size in patients with solitary autonomous functioning toxic thyroid nodules.
Clin Endcrinol 1999;49:197-202. - Laurberg P, Pedersen KM, Hreidarsson A, Sigfusson N, Iversen E, Knudsen PR.
Iodine intake and the pattern of thyroid disorders: a comparative epidemiological study of thyroid abnormalities in the elderly in Iceland and in Jutland, Denmark.
J Clin Endocrinol Metab. 1998 Mar;83(3):765-9. - Bahn RS, Burch HB, Cooper DS, Garber JR, Greenlee MC, Klein I, Laurberg P, McDougall IR, Montori VM, Rivkees SA, Ross DS, Sosa JA, Stan MN; American Thyroid Association; American Association of Clinical Endocrinologists.
Hyperthyroidism and other causes of thyrotoxicosis: management guidelines of the American Thyroid Association and American Association of Clinical Endocrinologists.
Endocr Pract. 2011 May-Jun;17(3):456-520.
Supplerende oversigt:
Franklyn JA, Boelaert: Thyrotoxicosis. Lancet 2012; 379;1155-1166.
